
焦虑症是全球高发的精神疾病,全球患病率约 3.3%,给社会经济带来沉重负担。一线血清素能药物存在副作用、依赖风险及长期疗效不稳定等问题,亟需更安全有效的干预方式。
呼吸与情绪存在固有关联,焦虑常伴随呼吸异常(如呼吸急促、睡眠呼吸暂停),而深呼吸、瑜伽等呼吸干预已被证实可缓解焦虑,但背后的神经环路机制尚未明确。

2026年3月2日,河北医科大学袁芳/王升/上海交通大学袁逖飞在国际知名期刊Advanced Science发表题为:Respiratory-Limbic Coupling via a Thalamic Circuit Alleviates Anxiety的研究。
核心发现:本研究以雄性小鼠和人类为研究对象,发现呼吸中枢preBötC谷氨酸能神经元(preBötCGlu)→丘脑室旁核(PVT)→中央杏仁核(CeA)是调控焦虑与呼吸的保守神经环路:激活该环路可显著缓解急性束缚应激(ARS)诱导的焦虑样行为及呼吸频率(RF)异常,抑制则加剧症状;其机制为 PVT 通过分别投射至 CeA 的外侧亚核(CeL)和内侧亚核(CeM)实现双向调控:PVT→CeL 通路发挥抗焦虑作用,PVT→CeM 通路促焦虑;
先前及最近的研究表明,小鼠的焦虑样表型与特定的呼吸模式改变(如梳理时间延长和呼吸频率升高)密切相关。
ARS应激诱导小鼠出现具有时间依赖性的焦虑行为与呼吸异常
本研究利用ARS模型诱导雄性小鼠产生焦虑,主要发现如下:
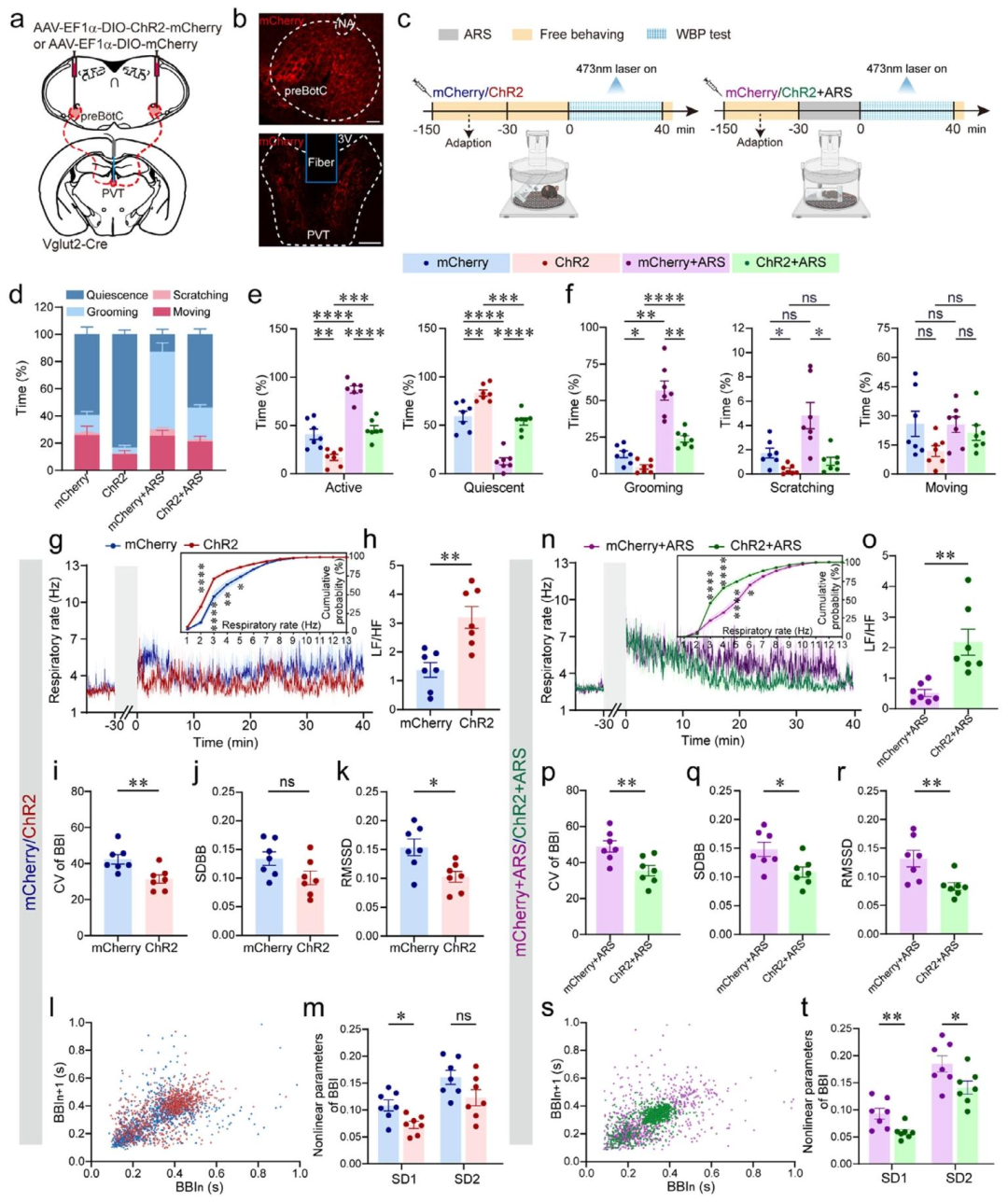
行为表现:ARS小鼠在应激后早期(0-10分钟)和中期(30-40分钟)表现出显著的焦虑行为(如在旷场箱中心和高架十字迷宫开放臂的活动减少),且活跃状态(梳理、抓挠、移动)时间延长,静止时间减少。这些症状在60-70分钟后恢复正常,显示具有时间依赖性。
呼吸动态监测显示,ARS小鼠出现应激性呼吸急促(RF升高),且呼吸频率变异性显著增加。具体表现为低频/高频比值降低,呼吸间期的短期变异性(SD1、RMSSD)增强,但长期变异性未变。

preBötCGlu→PVT→CeA 是核心神经环路
通过神经示踪和化学遗传学验证,preBötCGlu可通过PVT中继,间接投射至 CeA,且PVT中同时接收preBötC输入并投射至CeA的神经元密度显著高于其他核团(如NTS、LC、PBN)。
激活环路可缓解焦虑样行为及呼吸异常,环路抑制会恶化焦虑与呼吸功能,PVT→CeA 是环路的关键下游通路。
膜片钳记录显示,PVT对CeL神经元以兴奋性投射为主(58.8%),对CeM神经元以抑制性投射为主(57.1%),这种差异性投射是双向调控的核心机制。
慢呼吸特异性抑制杏仁核β/γ振荡以缓解人类焦虑
大量证据表明慢呼吸可缓解焦虑,但其神经机制尚不明确。基于此前小鼠研究(preBötC→PVT→CeA回路),本研究进一步揭示了人类慢呼吸的作用:
78名志愿者进行5分钟自主慢呼吸(4-7次/分)后,贝克焦虑量表(BAI)评分显著低于正常呼吸组。
杏仁核颅内记录显示,焦虑水平与全频段振荡功率正相关;慢呼吸特异性抑制β和高频γ波,该效应即时且持久且基线功率越高,抑制越强。
慢呼吸通过特异性调节杏仁核的β和高频γ振荡来减轻焦虑,且效果受基线活动水平影响,证实杏仁核是其中的关键神经基质。

本研究聚焦呼吸与焦虑的神经环路机制,通过动物实验与人体研究相结合,首次阐明preBötCGlu→PVT→CeA通路在呼吸-情绪整合中的核心作用,为焦虑障碍的非药物干预提供了全新的科学依据。
研究意义
首次揭示呼吸调控焦虑的核心神经环路,将传统呼吸干预从经验性实践提升为机制明确的环路调控策略。
为焦虑障碍提供了全新的治疗靶点(如 PVT→CeL 通路、CeA 亚核),推动生物电子疗法或精准呼吸干预方案的开发。
DOI: 10.1002/advs.202517477

欢迎转发分享

































热门跟贴