来源:市场资讯
(来源:Scientific Services和元生物)
PM2.5可通过呼吸道进入人体,部分研究表明其可能通过血液循环或直接接触影响口腔组织,引发或加重牙周炎症状,如牙龈炎症、牙槽骨吸收等。牙龈成纤维细胞(gingival fibroblast)是维持牙龈组织结构和功能的关键细胞类型。PM2.5暴露可能通过诱导氧化应激、炎症反应等,导致牙龈成纤维细胞损伤,表现为细胞形态改变、功能异常或细胞死亡。铁死亡是铁依赖性的程序性细胞死亡方式,已有研究证实铁死亡参与牙周炎进展,但 PM2.5 是否通过诱导牙龈成纤维细胞铁死亡加重牙周炎,其分子机制尚未明确。
2026年2月7日,中山大学附属口腔医院余东升/赵玮研究团队在Environment International发表题为Multi-omics reveals ferroptosis as a key mechanism in PM2.5-exacerbated periodontitis via gingival fibroblast damage的研究成果。
该研究通过细胞学实验结合多组学整合分析(转录组+代谢组),明确了铁死亡可能是 PM2.5 加重牙周炎的关键分子机制。PM2.5 被牙龈成纤维细胞内吞后,通过诱导细胞内铁蓄积、脂质过氧化过度产生,同时破坏线粒体稳态、激活炎症反应,最终触发牙龈成纤维细胞铁死亡,导致细胞活力、迁移能力下降,牙周组织稳态失衡,进而加重牙周炎进展;而铁死亡抑制剂 Fer-1 可有效阻断这一过程,逆转 PM2.5 诱导的牙龈成纤维细胞损伤。该研究建立了环境 PM2.5 暴露与牙周炎加重的分子关联,为空气污染相关牙周病的防治提供了新的作用靶点(如铁死亡关键分子 GPX4、ACSL4),也为开发针对性的牙周炎干预策略提供了实验依据。

·研究结果·
1. PM2.5 对牙龈成纤维细胞产生剂量依赖性毒性损伤
PM2.5 可被牙龈成纤维细胞内吞并定位于细胞质,且随浓度升高(≥ 50μg/mL),细胞活力显著下降,48h 时 100μg/mL PM2.5 组细胞活力抑制率达 41.1%,细胞出现皱缩、黏附密度降低等形态异常。

PM2.5 显著抑制牙龈成纤维细胞的迁移能力,划痕实验和 Transwell 实验显示,100μg/mL PM2.5 组细胞划痕闭合率、跨膜迁移细胞数显著降低,且迁移相关基因(钙粘蛋白、整合素 α、CXCL13、CXCR4)表达下调。

2. PM2.5 诱导牙龈成纤维细胞炎症激活并破坏线粒体稳态
炎症反应激活:PM2.5 处理后,促炎因子 IL-6、iNOS、MMP8 表达呈剂量依赖性升高,抗炎因子 TGF-β、Annexin A1 表达显著降低,提示牙龈成纤维细胞发生促炎重编程。

线粒体功能紊乱:PM2.5 导致线粒体膜电位显著去极化,线粒体 ROS 和细胞总 ROS 大量蓄积;线粒体融合相关蛋白(MFN1/2、OPA1)表达下调,分裂相关蛋白 Drp1 表达上调,线粒体质量控制相关分子(KIF5B、PGC1α、VDAC1)表达降低,线粒体融合 / 分裂动态平衡被打破。

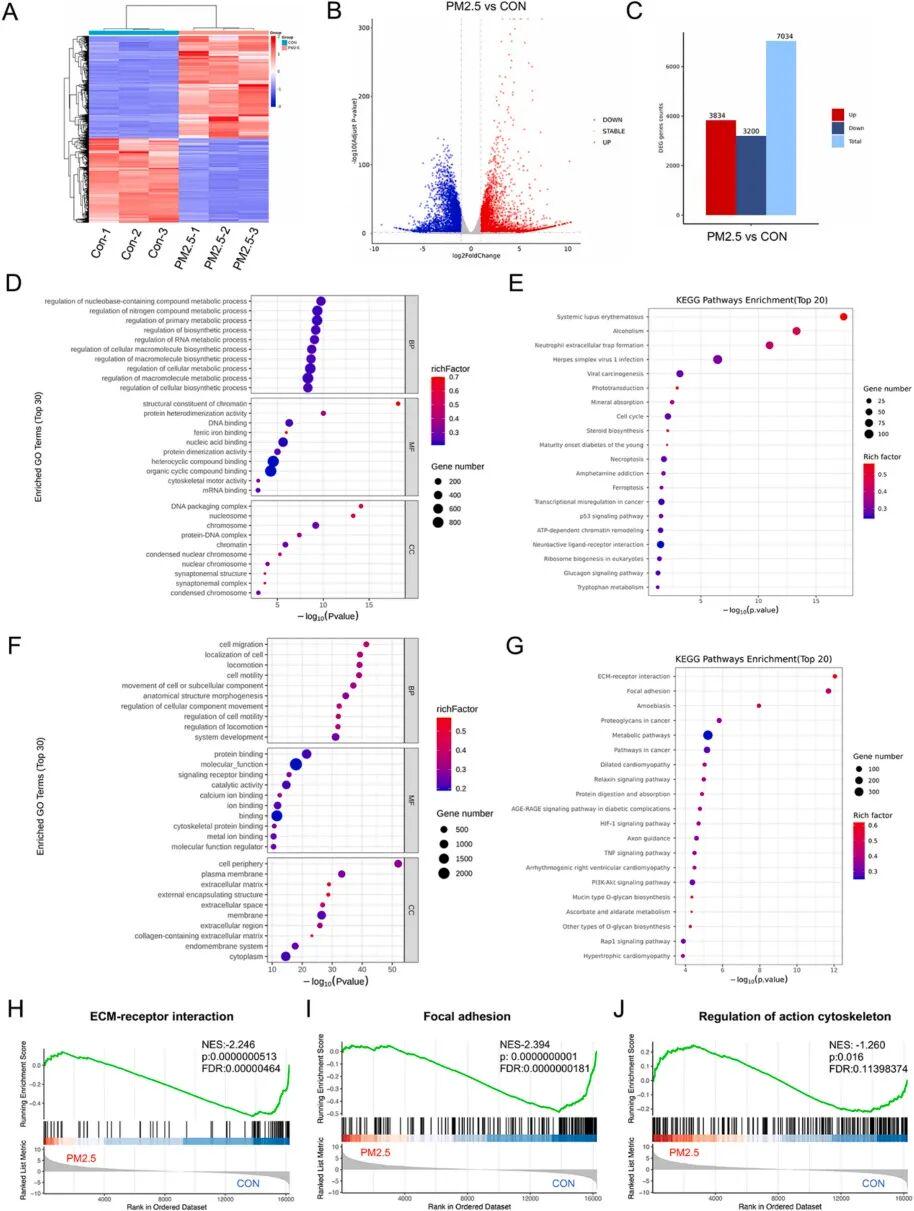
3.转录组揭示 PM2.5 诱导牙龈成纤维细胞的表达特征
共鉴定出 7034 个差异基因(DEGs),其中 3834 个上调表达,3200 个下调表达,两组表达谱差异显著。GO 富集分析表明,上调 DEGs主要参与铁离子结合、染色质重塑等过程,如various metabolic process、ferric iron binding、cytoskeletal motor activity、DNA packaging complex 和nucleosome。KEGG 富集分析表明,上调 DEGs主要参与通路为铁死亡和 ATP 依赖性染色质重塑,如ferroptosis、ATP-dependent chromatin remodeling。
GO 富集分析表明,下调 DEGs主要参与细胞迁移、细胞黏附等生物学过程,如cell migration、cell motility、calcium ion binding、cytoskeletal protein binding、plasma membrane、extracellular matrix。KEGG 富集分析表明,下调 DEGs主要参与通路为ECM、黏着斑、PI3K-Akt 信号通路,如ECM-receptor interaction、focal adhesion、PI3K-Akt signaling。
4.代谢组揭示 PM2.5 诱导牙龈成纤维细胞的代谢重编程
共鉴定出 261 个差异表达代谢物(DEMs),其中 136 个上调,125 个下调,主要包括75个脂质及类脂分子(32.19%)、56个有机酸及其衍生物(24.03%)、38个organoheterocyclic compounds(16.31%)。KEGG 通路富集显示,DEMs 主要参与铁死亡(ferroptosis)、谷胱甘肽代谢(glutathione metabolism)、精氨酸生物合成(arginine biosynthesis)、甘油磷脂代谢(glycerophospholipid metabolism),其中谷胱甘肽代谢紊乱与抗氧化防御系统受损相关,甘油磷脂代谢异常与脂质过氧化密切相关。

5. PM2.5 诱导铁死亡进而引起牙龈成纤维细胞损伤,但铁死亡抑制剂Fer-1 可有效挽救
PM2.5 处理后,牙龈成纤维细胞内 Fe²+ 大量蓄积,脂质过氧化水平显著升高,铁死亡关键分子发生特征性变化:促铁死亡分子 ACSL4、TFRC、COX2 表达上调,抗铁死亡分子 GPX4、SLC7A11 表达下调。
铁死亡抑制剂 Fer-1 可显著抑制 PM2.5 诱导的脂质过氧化、Fe²+ 蓄积和 ROS 生成,逆转 PM2.5 对细胞活力、增殖的抑制作用,减少细胞死亡;而凋亡、焦亡等其他细胞死亡方式的抑制剂虽也有一定保护作用,但铁死亡是 PM2.5 诱导牙龈成纤维细胞损伤的核心机制。

原文链接:https://www.sciencedirect.com/science/article/pii/S0160412026000978
和元助力
和元生物有幸为研究者提供转录组测序(RNA seq)服务,以实际行动助力基础科学研究!
和元生物多组学服务
和元生物提供多组学服务(如转录组、蛋白组、代谢组、微生物组等)和单细胞及空间转录组服务(如10x Genomics GEM-X单细胞转录组(v4.0)、10x Genomics单细胞转录组(v3.1)、10x单细胞转录组及TCR/BCR、墨卓单细胞转录组、DNBelab C-TaiM4单细胞转录组、10x HD空间转录组等),致力于为广大生命科学家、医学工作者提供基于多组学的科研及临床应用解决方案。累计协助客户在Advanced Functional Materials、ACS Nano、Nature Aging、Cancer Research、Neuron、Advanced Science、Experimental & Molecular Medicine、Journal of Nanobiotechnology、Cell Death and Disease等期刊发表SCI论文,并推出了广受好评的生信分析云平台【https://analysis.obiosh.com/】,助您高效实现个性化数据挖掘!
精彩合集
和元生物
和元生物成立于2013年,作为深耕细胞和基因治疗核心领域的高新技术企业,专注于为细胞和基因治疗的基础研究提供基因治疗载体研制、基因功能研究、药物靶点及药效研究等CRO服务,可提供①组学服务:常规转录组、单细胞转录组、基因组、代谢组及蛋白组等。②载体构建和病毒包装:质粒、siRNA、腺相关病毒(AAV)、腺病毒(ADV)、慢病毒(LVV)、逆转录病毒(RV)、单纯疱疹病毒(HSV)等病毒载体生产服务,提供R&D、实验室级别、GMP级别满足研发、小动物、大动物NHP到临床的不同研究阶段的使用需求。③细胞实验服务:过表达、干扰稳定株构建,单克隆细胞株构建服务及细胞功能学、药效学实验服务。④动物实验及机制研究:神经、代谢、肿瘤动物模型、药效药代、病理切片及蛋白、核酸检测服务。⑤特色项目服务:CRISPR文库筛选服务,外泌体整体研究服务,AAV衣壳筛选服务、听力研究整体项目服务,满足客户定制化或一站式项目服务,助力基础科学研究,促进基础研究到临床转化应用,推动细胞和基因治疗行业发展。



























热门跟贴