来源:市场资讯
(来源:求实药社)
3 月 4 日,药物临床试验登记与信息公示平台官网显示,阿斯利康登记了一项特泽利尤单抗(Tezepelumab)用于鼻内镜下鼻息肉评分 ≥4 分慢性鼻窦炎伴鼻息肉成人患者附加维持治疗的 IIIb 期临床研究(BIFANG)。

打开网易新闻 查看精彩图片
药物临床试验登记与信息公示平台官网
BIFANG 研究是一项多中心、单臂、IIIb 期临床试验,旨在评估鼻内镜评分 ≥4 分的中国慢性鼻窦炎伴鼻息肉成人受试者使用特泽利尤单抗治疗后鼻息肉评分及症状改善情况。用药方案为每 4 周皮下注射一次,合计 24 周。
该研究计划在国内入组 230 名受试者,主要终点是描述鼻息肉评分(NPS)相较基线的变化情况,以及描述受试者报告的鼻塞情况(NCS)相较基线的变化情况。
特泽利尤单抗是一款靶向胸腺基质淋巴细胞生成素(TSLP)的单克隆抗体。通过精准阻断 TSLP,特泽利尤单抗可从源头抑制相关炎症通路激活,从而缓解疾病症状。
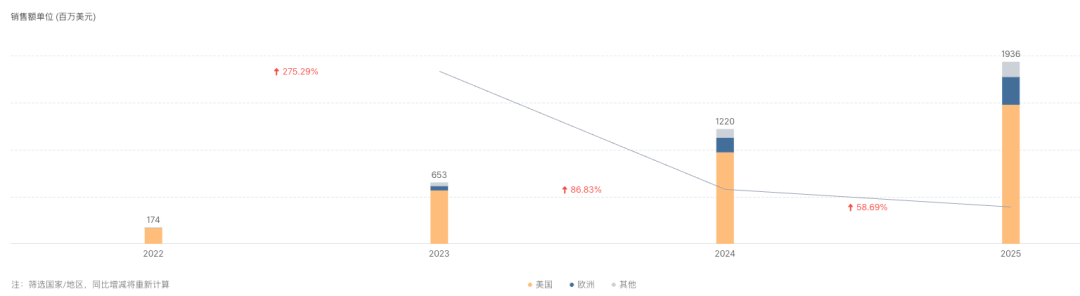
目前,特泽利尤单抗已经在美国、日本、欧盟获批 2 项适应症,分别是哮喘、慢性鼻窦炎伴鼻息肉病。从市场表现来看,该产品增长强劲, 2024 年全球销售收入达到 12.20 亿美元,同比增幅高达 87%,2025 年进一步增长至 19.36 亿美元。
打开网易新闻 查看精彩图片
文章内容仅供参考,不构成投资建议。投资者据此操作,风险自担, 关于对文中陈述、观点判断保持中立,不对所包含内容的准确性、可靠性或完整性提供任何明示或暗示的保证。请读者仅作参考,并请自行承担全部。





























热门跟贴