酰胺键,是现代药物分子中出现频率最高的化学键之一。统计显示,在2023年全球销量排名前200的小分子药物中,有117种至少包含一个酰胺键,几乎覆盖了抗肿瘤、心血管、抗感染等所有重要治疗领域。然而,正是这样一个“基础到不能再基础”的结构单元,却长期依赖并不理想的合成方式。在传统化学合成中,酰胺键的构建往往需要将羧酸“激活”为高能中间体,并配合大量缩合试剂才能完成偶联。这不仅步骤繁琐、原子经济性低,还会产生大量副产物和化学废物,成为制药工业中碳排放和成本的重要来源。尽管近年来不断有改良策略出现,但要在反应效率、底物普适性、环境友好性之间同时取得突破,仍然极具挑战。相比之下,自然界的酶体系在温和条件下高效、选择性地构建化学键,提供了另一种可能。然而,现有的酶促酰胺合成策略,大多仍然围绕“羧酸活化”展开,尚未真正跳出传统反应逻辑。能否从更低活性的前体出发,用生物催化的方式直接构建酰胺键?这是一个长期悬而未决的问题。
今日,北京大学雷晓光教授提出了一种全新的生物催化策略:通过蛋白工程手段,将自然界中广泛存在的醛脱氢酶(ALDH)重新设计为一种全新的“氧化酰胺化酶”(OxiAm),实现了醛与胺在水相条件下直接生成酰胺键。该反应以空气中的氧作为唯一氧化剂,不需要任何缩合试剂,在温和条件下即可进行。更进一步,研究团队将该体系与醇脱氢酶和辅酶循环模块相结合,构建出从醇出发的一锅式酶促级联反应,直接合成多种药物相关酰胺分子。该策略展现出优异的底物适应性、官能团耐受性和放大潜力,为绿色制药提供了一条全新的合成路径。相关成果以“Engineered aldehyde dehydrogenases for amide bond formation”为题发表在《Science》上, Lei Gao、Xiang Qiu、Jun Yang和Kangdelong Hu为共同第一作者。
尤其值得一提的是,雷晓光教授团队的相关成果于昨日刚刚发表于《Nature》,今日又在《Science》报道最新进展。

雷晓光教授


从传统路径到新思路
研究的起点,来自对酰胺键构建路径的重新审视。如图1a所示,当前主流的化学和酶促方法,几乎都建立在“高活化羰基化合物”之上——羧酸、酯或腈必须先被激活,才能与胺发生偶联。而近年来出现的氧化酰胺化反应,虽然在概念上更简洁,却往往依赖贵金属或有毒催化剂,限制了实际应用。研究团队注意到,醛脱氢酶在自然反应过程中,会经历一个高度活泼的硫酯中间体(图1b)。在野生型酶中,这一中间体会迅速被水分子进攻,生成羧酸。但如果能阻止水的进入,同时让胺分子优先参与反应,就有可能在不经过羧酸活化的情况下,直接生成酰胺键。这一看似“反直觉”的设想,成为整项工作的核心突破口。

图1:传统酰胺键合成路径与酶促氧化酰胺化新策略对比
结构导向的酶工程改造
为了验证这一思路,研究团队以一种来源于假单胞菌的醛脱氢酶为模型,对其活性中心进行了系统性分析(图2a)。晶体结构显示,多个高度保守的亲水氨基酸残基在活性口袋中共同作用,促进水分子进入并完成水解。通过定点突变和组合突变策略,研究者逐步替换这些关键残基,使活性口袋变得更加疏水且空间更大(图2b)。这一改变显著削弱了水解路径,同时增强了胺分子的结合能力。X射线晶体学进一步证实,改造后的酶结构成功稳定了胺进攻硫酯中间体的构象,为酰胺键形成提供了结构基础。最终获得的OxiAm变体,在多种条件下均能以酰胺为主要产物,标志着醛脱氢酶功能的根本性转变。

图2:醛脱氢酶活性口袋的结构改造与机制解析
广泛底物与高选择性
在反应性能测试中,OxiAm展现出令人印象深刻的通用性。如图3所示,无论是芳香醛、杂环醛,还是脂肪族醛,都能与多种一、二级胺顺利反应,生成对应的酰胺产物。更重要的是,反应对羟基、羧基、酯基、双键等官能团高度耐受,极大降低了后续保护–脱保护操作的需求。对于传统方法中反应性较低的芳香胺,研究团队还通过进一步精细化改造酶的“胺通道”,显著提升了反应效率,使得多种药物级芳香酰胺得以高效合成。
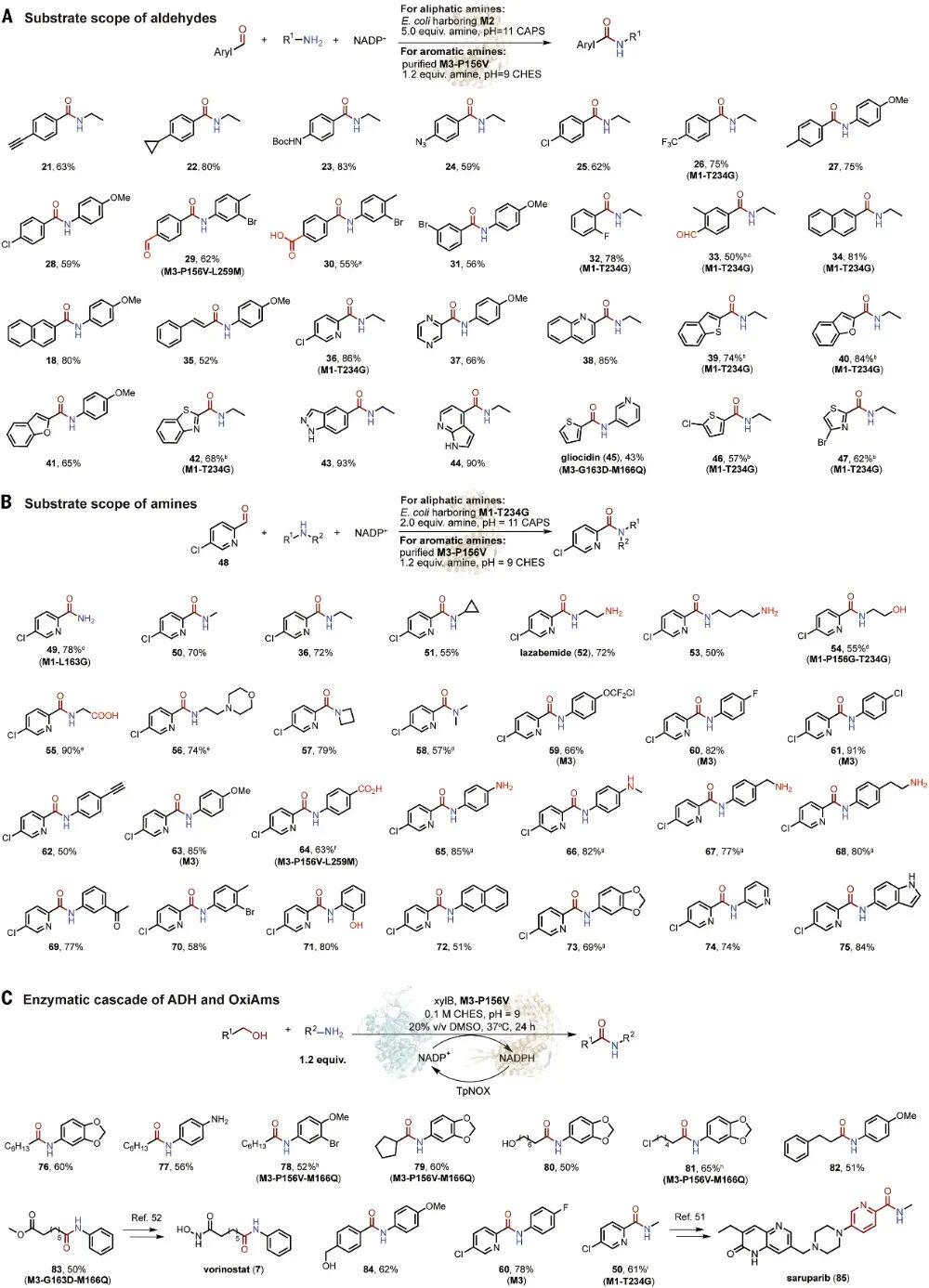
图3:OxiAm对不同醛和胺底物的适用性展示
从醇直接出发的酶促级联
考虑到脂肪族醛的不稳定性,研究团队进一步将OxiAm与醇脱氢酶和辅酶再生系统整合,构建出一套完全酶促的级联反应体系(图4a)。在该体系中,醇首先被氧化为醛,随后在同一反应体系中直接转化为酰胺,实现真正意义上的“一锅法”。该策略被成功应用于多种药物分子和关键中间体的合成,包括抗肿瘤和神经系统药物相关结构。在克级放大实验中,体系依然保持稳定的转化率和选择性,展示出良好的工业化潜力(图4b–d)。

图4:从醇直接合成酰胺的酶促级联反应及药物应用示例
小结
这项研究的价值,并不仅在于提供了一种新的酰胺键合成方法。更重要的是,它展示了一种具有普适意义的策略:通过精确的蛋白工程,重新定义天然酶的反应结局。由于醛脱氢酶在自然界中分布极广,研究中提出的改造原则已被证明可推广至多种同源酶,为构建新的生物催化反应网络提供了坚实基础。未来,随着酶工程和计算设计手段的进一步发展,这类“功能重编程”的生物催化剂有望在绿色制药、精细化工乃至材料合成领域发挥更大作用。





























热门跟贴