作者:闵
提起贝伐珠单抗,想必广大病友都不陌生。无论是服用靶向药,还是接受化疗或免疫治疗的患者中,都不乏正在联合使用贝伐珠单抗的例子。
作为最常见的抗血管生成类药物,贝伐珠单抗广泛应用于抗癌治疗,也频繁出现在各类联合用药方案中。
不少病友好奇它究竟能为治疗带来多大帮助,本文便围绕贝伐珠单抗与各类方案联合的疗效展开探讨。
1
贝伐珠单抗是个什么药?
贝伐珠单抗(后简称“贝伐”)虽名为“单抗”,但与当前备受关注的另一类“单抗”不同,它并不属于免疫抑制剂。
贝伐以血管内皮生长因子(VEGF)为作用靶点,通过抑制VEGF的活性来阻碍肿瘤新生血管的生成,从而抑制肿瘤获取营养,达到抗肿瘤的效果。
因此,贝伐属于抗血管生成药物,是该类药物中最早面世的成员,与之同属这一家族的还有安罗替尼、仑伐替尼等口服小分子激酶抑制剂(此处不再赘述)。

自上市以来,贝伐已斩获多个癌种的适应症,在临床上广泛应用于结直肠癌、非小细胞肺癌、肾细胞癌、卵巢癌及宫颈癌等多种癌症,堪称“万金油”和“多面手”。
尽管应用广泛,贝伐多与化疗、靶向治疗等方案联合使用,那么其联合效果究竟如何呢?
2
贝伐珠单抗的各种联合方案效果如何?
1
贝伐 + 靶向药
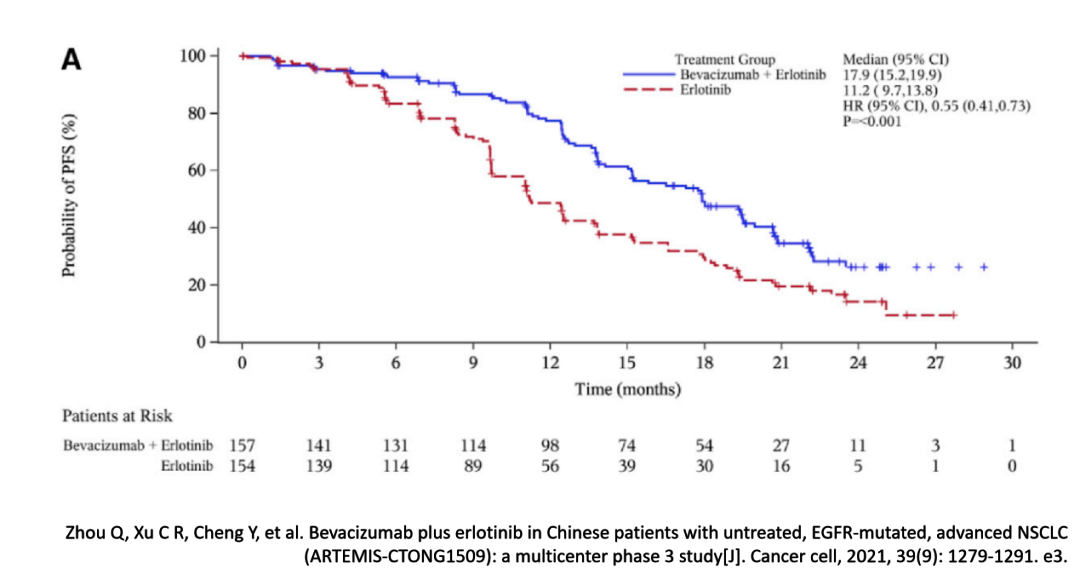
贝伐与靶向药联合使用的案例众多,我们以较为经典的“贝伐 + 厄洛替尼(特罗凯)”的“A+T”方案为例进行说明。ARTEMIS-CTONG1509研究将携带EGFR突变的非小细胞肺癌患者分为两组,一组采用“A+T”方案,另一组则单用厄洛替尼(即“T”)治疗[1]。
结果显示,A+T组的中位无进展生存期(PFS)显著长于单T组(17.9个月 vs 11.2个月);A+T组的中位总生存期(OS)略长于单T组,但无统计学差异(36.2个月 vs 31.6个月)。
在副作用方面,A+T组发生3级及以上不良反应(含所有类型)的比例为54.8%,而单T组为26.1%。
2
贝伐 + 化疗
“培美曲塞 + 铂类 + 贝伐”的联合方案在肺腺癌患者中十分常见,我们以此为例探讨贝伐联合化疗的疗效。
2025年,我国一项名为BAP BRAIN的研究对比了贝伐联合化疗与单纯化疗在脑转移非鳞非小细胞肺癌患者中的疗效[2]。
结果显示,联合组的中位PFS长于化疗组(11.07个月 vs 7.37个月);联合组的中位OS略长于化疗组,但仍无统计学差异(28.07个月 vs 18.53个月)。
联合组发生各类3级及以上不良反应的比例为34.2%,而化疗组为24.3%,且联合组出现高血压、蛋白尿、血栓及出血等特异性副作用的比例更高。
2021年,另一项综合4项研究的meta分析也得出类似结果:联合组可显著延长中位PFS,但对OS的改善有限[3]。
3
贝伐 + 免疫治疗 + 化疗
2023年,日本发表的一项研究探索了“T药”(阿替利珠单抗)+ 含铂化疗联合或不联合贝伐的疗效差异[4]。
结果表明,联合贝伐组的中位PFS略高于不联合组,但无统计学差异(9.6个月 vs 7.7个月);联合贝伐组的中位OS也略高于不联合组,同样无统计学差异(29.4个月 vs 25.3个月)。两组发生各类3级及以上不良反应的比例相近(55% vs 57%)。

T药属于PD-L1抑制剂,那么贝伐联合PD-1抑制剂是否会有所不同?
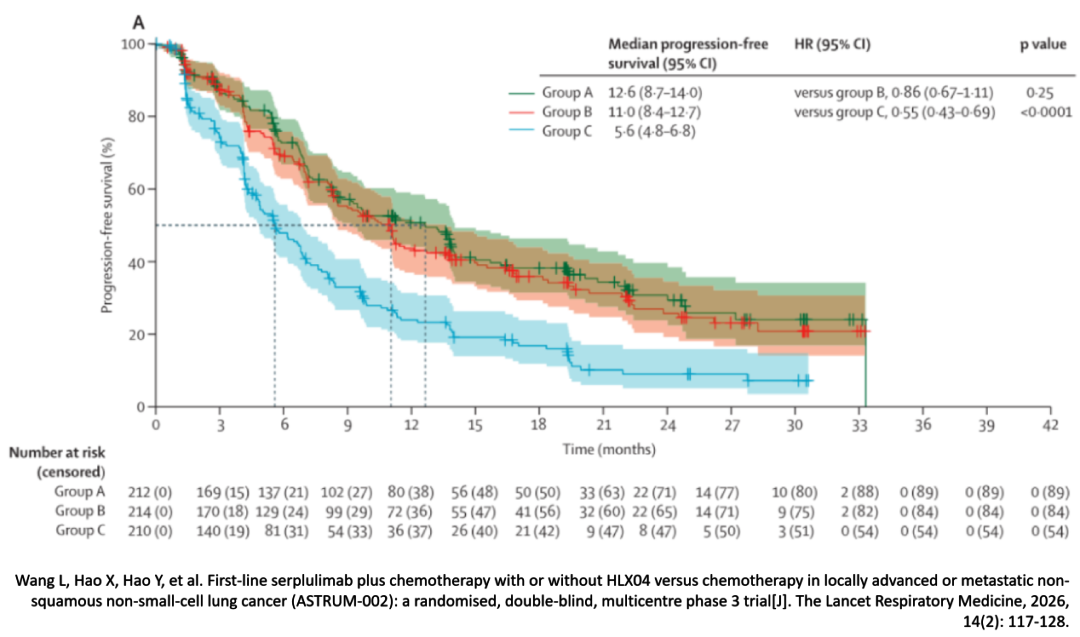
石远凯教授团队最新发表的ASTRUM-002研究可以回答这一问题。
该研究采用斯鲁利单抗联合化疗,并在此基础上联合一种贝伐类似物,将患者分为三组,分别接受三药联合方案、免疫+化疗方案以及单纯化疗方案[5]。
结果显示,三药联合组的中位PFS虽略长于免疫+化疗组,但无统计学差异(12.6个月 vs 11.0个月),化疗组在三组中疗效最差。
同时,三药联合组的3级及以上不良反应发生率为71%,免疫+化疗组为66%,化疗组为57%。
贝伐不愧为“万金油”,无论是与化疗、靶向治疗还是免疫治疗联合,均能实现“混搭”,且疗效表现一致,在联合治疗期间均能显著延长中位PFS(即通常所说的耐药时间)。
然而,细心的病友可能会疑惑:上述联合方案似乎并未最终带来明确的总生存期提升,这该如何理解?
除研究中的方案耐药后存在交叉用药、不联合组后续也可选择贝伐、化疗、免疫治疗及靶向治疗等因素外,特定的临床特征也会影响联合用药的获益情况。

图片来源:包图网
3
狐假虎威还是悄悄的偏袒?
总体而言,贝伐联合各类治疗方案均能显著延长中位PFS,即联合方案的整体耐药时间均长于未联合组。尽管联合组的中位OS均呈现优于未联合组的趋势,但均未达到统计学显著性。
这难免让病友担心这种获益如同“镜花水月”,怀疑贝伐只是一个“狐假虎威”的角色。
然而,在大家忽略的细节中,实则隐藏着为贝伐“正名”的证据——它并非“狐假虎威”,而是在平等增效的前提下,对某些特殊人群表现出明显的“偏爱”。
接下来,我们看看哪些特征的患者更容易从联合方案中获益。
1
脑转移患者
CTONG1509研究中,无论是否存在脑转移,A+T组的中位PFS均优于T组。值得关注的是,在脑转移人群中,A+T组的中位OS也显著长于T组,即脑转移患者在使用靶向药的同时联合贝伐,可进一步提升疗效。
贝伐不仅在联合靶向药时表现如此,在联合化疗时同样如此。前文提到的BAP BRAIN研究纳入的全部为脑转移患者,亚组分析发现,化疗联合贝伐更能延长多发脑转移(≥4个病灶)或最大病灶≤1 cm患者的中位OS。
上述证据表明,贝伐具有增强颅内疗效的作用,且这一作用无论与靶向药还是化疗联合均可发挥。
2
EGFR L858R人群
CTONG1509研究中,在EGFR L858R突变人群中,A+T组的中位PFS获益更为明显(19.5个月 vs 9.7个月),而在EGFR 19Del人群中获益相对不明显(17.7个月 vs 12.5个月)。
遗憾的是,A+T组相较于T组并未延长EGFR L858R人群的中位OS(33.8个月 vs 34.9个月)。这可能与A+T组耐药后接受后续治疗的比例低于单药组有关,并不完全由联合方案决定。
此外,目前多项证据表明,EGFR L858R人群在接受相同靶向药物治疗时,其疗效通常劣于19Del人群。结合CTONG1509研究的发现,这部分患者为增强一线治疗疗效,可考虑在此时联合贝伐。
3
PD-L1高表达
在不少病友的印象中,PD-L1高表达意味着可以单独使用免疫治疗,从而摆脱化疗。
然而,ASTRUM-002研究发现,对于PD-L1高表达的患者,若在免疫联合化疗的基础上再加用贝伐类似物,获益更为显著。
三药联合组的中位PFS达27.2个月,显著长于免疫+化疗组的12.1个月。我们期待该研究后续公布包括OS在内的更多数据,进一步明确三药联合能否将如此显著的中位PFS获益转化为最终的总生存期获益。

图片来源:包图网
4
总结
贝伐珠单抗作为较早上市的抗血管生成药物,在当前治疗中应用极为广泛,常与靶向药、化疗及免疫治疗等联合使用。
作为“万金油”,贝伐很好地完成了自身任务,与各类药物联合时均能提升中位PFS等临床疗效指标。
贝伐的作用并非“开天辟地”式的显著,例如其对总生存期的提升有时未达理想水平;然而,它在联合治疗中的价值体现在细节之中——既能为整体人群带来获益,又能对部分具有特定临床特征的患者提供更显著的优势。
因此,各位病友无需盲目追求联合用药。用药越多,相应的副作用也会越多,且贝伐仍可在后线治疗中使用。建议结合自身实际情况,做出合理决策。
参考文献
[1] Zhou Q, Xu C R, Cheng Y, et al. Bevacizumab plus erlotinib in Chinese patients with untreated, EGFR-mutated, advanced NSCLC (ARTEMIS-CTONG1509): a multicenter phase 3 study[J]. Cancer cell, 2021, 39(9): 1279-1291. e3.
[2] Li M, Pan Y, Jiang G, et al. Bevacizumab plus chemotherapy versus chemotherapy in untreated advanced non-squamous non-small-cell lung cancer patients with brain metastases (BAP BRAIN): an open-label, randomized, multicenter, phase III study[J]. ESMO open, 2025, 10(12): 105908.
[3] Garon EB, Peterson P, Rizzo MT, Kim JS. Overall Survival and Safety With Pemetrexed/Platinum ± Anti-VEGF Followed by Pemetrexed ± Anti-VEGF Maintenance in Advanced Nonsquamous Non-Small-Cell Lung Cancer: A Pooled Analysis of 4 Randomized Studies. Clin Lung Cancer. 2022 May;23(3):253-263.
[4] Shiraishi Y, Kishimoto J, Sugawara S, et al. Atezolizumab and Platinum Plus Pemetrexed With or Without Bevacizumab for Metastatic Nonsquamous Non-Small Cell Lung Cancer: A Phase 3 Randomized Clinical Trial. JAMA Oncol. 2024 Mar 1;10(3):315-324.
[5] Wang L, Hao X, Hao Y, et al. First-line serplulimab plus chemotherapy with or without HLX04 versus chemotherapy in locally advanced or metastatic non-squamous non-small-cell lung cancer (ASTRUM-002): a randomised, double-blind, multicentre phase 3 trial[J]. The Lancet Respiratory Medicine, 2026, 14(2): 117-128.
1.
与癌共舞公众号及网站及APP上发表的文章及讨论仅代表作者或发帖人个人观点,不代表平台立场。
与癌共舞公众号文章经医学编辑和版主审核,具有明显谬误和不良引导的文章将禁止发表。































热门跟贴